生产追溯系统产品的上市凭证怎么操作啊?
fly
2025-03-27
次浏览
作者:fly
发布时间:2025-03-27
浏览次数:
生产追溯系统产品的上市凭证操作流程,会因行业、地区以及所使用的具体追溯 云表提供[生产追溯系统产品凭证]解决方案[18luck体育登录安卓版]

2025-03-27
生产追溯系统产品的上市凭证操作流程,会因行业、地区以及所使用的具体追溯系统不同而存在差异。
以下以食品、农产品行业为例,为你介绍通用的大致操作步骤:
以下以食品、农产品行业为例,为你介绍通用的大致操作步骤:
注册与入驻追溯平台:
确定适用平台:不同行业有其对应的权威追溯平台,例如食品行业,像福建省使用 “福建省食品生产经营追溯管理系统”,江苏省针对进口冷链食品启用 “江苏省进口冷链食品追溯系统” 。你需要依据所在地区及产品类别,明确应入驻的平台。
完成注册流程:访问追溯平台的官方网站或指定的注册入口,点击注册按钮,填写企业的相关信息,包括企业名称、统一社会信用代码、法定代表人姓名、地址、联系方式,以及生产经营许可证或备案等信息。部分平台还可能要求上传企业资质证明文件,如营业执照、生产许可证的扫描件,以完成实名认证与资质审核。注册完成后,获取平台分配的账号和密码,用于后续登录操作。
完善产品基础信息:
录入详细信息:登录追溯平台后,找到产品信息录入相关模块,一般在 “产品管理” 或类似菜单下。按要求填写产品的基本信息,涵盖产品名称、型号、规格、配料表(食品行业)、生产工艺简述、生产日期、保质期、储存条件等内容。对于农产品,还需补充种植 / 养殖环境信息、农药 / 兽药使用情况等。
上传证明文件:如有产品合格证明、第三方检验报告、质量认证证书(如有机食品认证、绿色食品认证等),需在系统指定位置上传这些文件的电子版,以证明产品质量符合相关标准,满足上市要求。
生成追溯码与凭证:
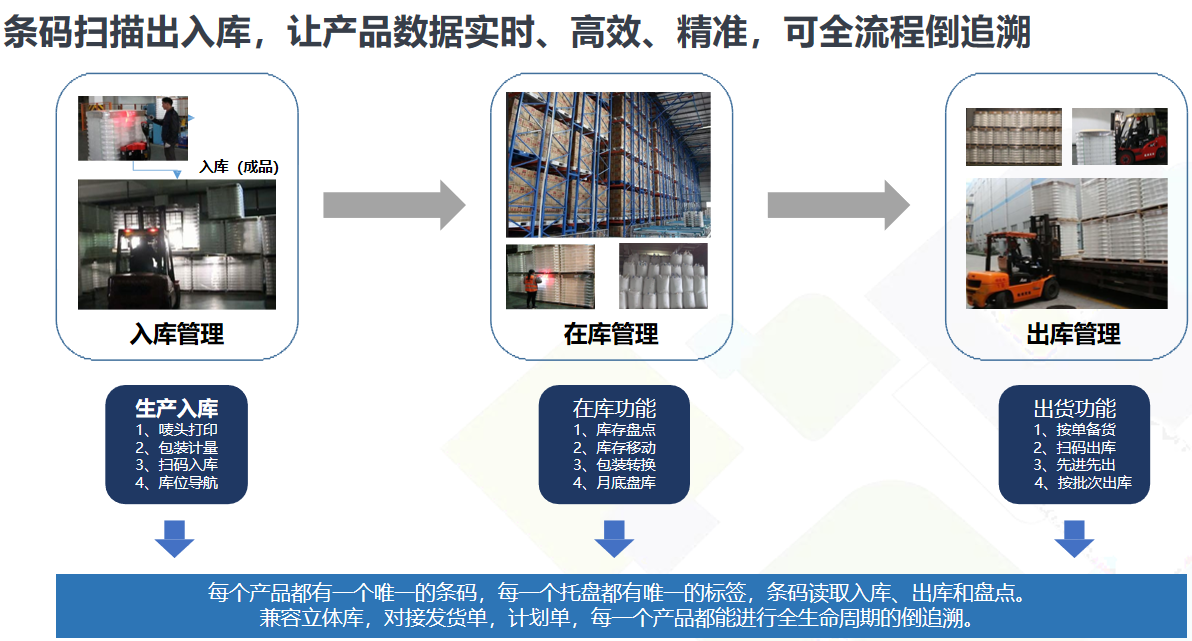
生产批次码生成:在产品完成生产产出或组合时,在追溯平台进行生产批次管理操作。系统会依据设定规则,自动生成与该产品生产批次相对应的唯一代码,即生产批次码。此代码可打印在产品追溯标识或追溯凭证上,常见的如二维码、条形码形式,方便后续扫码追溯信息。例如在农产品领域,农产品生产经营者在国家追溯平台完成生产批次管理后,就能获取相应的生产批次码 。
入市批次码获取(若有):若产品需进入特定市场环节(如批发市场、零售市场或生产加工企业),在平台填写详细的交易信息,包含交易双方信息、产品数量、交易日期等。提交后,系统生成对应该入市批次产品的入市批次码,打印在产品入市追溯凭证上 。
粘贴追溯码与凭证:
追溯码粘贴:将生成的追溯码以印刷或粘贴的方式,附着在产品包装、容器或附随标签标识的醒目位置,确保消费者或监管人员在购买、查验产品时能方便扫描查询。比如食品的预包装上,会在正面或侧面清晰粘贴追溯二维码。
追溯凭证留存与交付:打印出纸质的追溯凭证,详细记录产品从原材料采购到生产、检验等各环节信息。对于销售给下游经销商、零售商的产品,将追溯凭证随货同行交付;企业自身需留存一份电子和纸质档追溯凭证,以备监管部门检查及后续追溯查询使用。在福建省,进入农产品批发市场、大型商场等场所的食用农产品,就必须同时具备追溯二维码和追溯凭证 。
数据上传与维护:
及时上传生产数据:生产过程中,要实时或定期将生产环节数据录入追溯系统,包括原材料投入记录(原材料批次号、使用量等)、生产设备运行参数、各工序生产时间及操作人员、质量检验结果等。保证生产环节信息完整且与产品实际生产情况一致,为后续追溯提供详实依据。
更新产品流向数据:产品完成销售出库后,及时在追溯系统录入产品的销售流向信息,如客户名称、地址、联系方式、销售数量、销售日期、销售订单编号等。通过持续更新产品流向数据,实现产品从生产到销售终端的全流程追溯 。
在整个操作过程中,务必严格遵循所在地区相关法律法规以及追溯平台的规定要求,确保信息真实、准确、完整。若在操作上市凭证过程中遇到技术问题,可联系追溯平台的客服支持,获取针对性的指导与帮助 。
2025-03-27
上市凭证申报准备:从数据到证据的智能转化
当系统积累足够生产批次数据后,需按照目标市场的法规要求进行结构化数据整理。医疗器械企业申请CE认证时,需同步提交包含UDI编码、灭菌记录、生物相容性报告等在内的技术文档。
申报材料生成三步法:
1、资质核验
确认产品符合ISO 9001、HACCP等基础认证
检查检测机构是否具备CNAS、CMA资质(如某电子产品出口欧盟时,EMC检测必须由Notified Body完成)
2、数据筛选
按”时间戳+操作人员+设备编号”维度提取关键过程记录
运用系统内置的合规检查模块,自动识别缺失项(如某化工企业发现3%批次缺少催化剂添加记录)
3、报告生成
调用预设模板自动生成PDF版质量档案
支持添加数字签名与水印,防止文件篡改
三、电子化申报与动态维护:打造持续合规的闭环
随着各国推行电子政务,在线申报平台已成为主流渠道。我国药监局的eRPS系统可实现医疗器械注册电子提交,美国FDA的CDRH Portal则支持510(k)申请的全程数字化。
操作进阶技巧:
跨系统对接:通过API接口将追溯系统与监管平台直连,实现申报材料一键提交
智能预审:利用NLP技术解析法规文本,提前识别材料中的矛盾表述(如某企业规避了”灭菌保证水平SAL”与”无菌检验”的概念混淆风险)
动态更新:当生产工艺变更时,系统自动触发新版技术文档编制,确保上市后变更合规
值得关注的是,欧盟即将实施的EPR法规要求企业提供产品碳足迹追溯数据。某新能源企业通过升级追溯系统,成功在电池模组档案中嵌入原材料溯源图谱与能耗记录,率先获得EPR认证。
在实践过程中,企业常陷入两个误区:
一是过度追求系统功能完备性而忽视数据质量,导致申报时出现”有系统无证据”的窘境;
二是将追溯系统孤立运作,未与ERP、MES等系统打通形成数据闭环。
因此,建议在系统规划阶段就明确数据输出标准,并建立跨部门协作机制,让生产、质量、法规部门共同参与系统验证。
一是过度追求系统功能完备性而忽视数据质量,导致申报时出现”有系统无证据”的窘境;
二是将追溯系统孤立运作,未与ERP、MES等系统打通形成数据闭环。
因此,建议在系统规划阶段就明确数据输出标准,并建立跨部门协作机制,让生产、质量、法规部门共同参与系统验证。
你可能会喜欢
18luck体育登录安卓版 -->










.jpg)
.jpg)